O comportamento ondulatório foi criticada por diversos físicos da época, mas a ampliação de pontos de vista causada graças ao desenvolvimento da mecânica quântica fez com que a atitude da época fosse diferente. A ideia é que a radiação comporta-se como uma onda em certas ocasiões e como partícula em outras. Essa situação é colocada em evidência no trabalho experimental de Compton.
Primeiramente é necessário fazer algumas considerações.
Ondas são perturbações em um meio, transportando exclusivamente energia de um ponto a outro.
 |
| Gif: Wikipédia |
Após estudos sobre o efeito fotoelétrico e a quantização dos fótons, ficou determinado que estes fótons seriam simplesmente partículas, e foi então pela primeira vez que a luz que tem propriedades ondulatórias, também tem propriedades corpuscular, conhecido assim como dualidade onda-partícula.
Na tese de doutorado de Louis de Broglie, ao analisar que a luz tem essa propriedade dual, percebeu e questionou se outras matérias teriam tal propriedade. Tudo que existe em nossa volta seria dotado de comprimento de onda, amplitude e frequência, o que vai contra a nossa intuição. Anos depois essa hipótese foi posta a teste, através do experimento da fenda dupla, que consiste em emitir um feixe de luz contínuo em duas pequenas fendas separadas por certa distância.
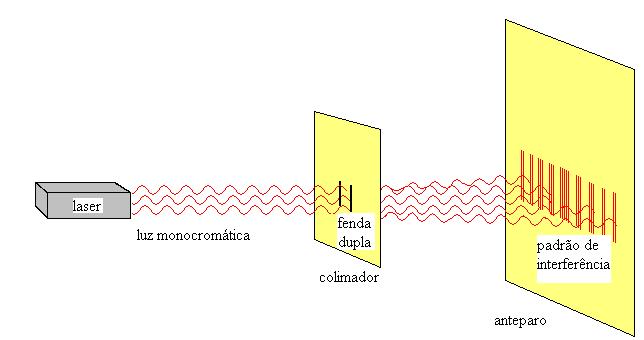 |
| Imagem: Infoescola |
O que foi observado era um padrão de máximos e mínimos, realizados através de difração e interferência, fenômenos de natureza ondulatória. Confirmando assim a hipótese de de Broglie e lhe rendendo o prêmio Nobel.
Você pode ser perguntar então o porque de não agirmos como uma onda, e a resposta é bem simples.
Em sua tese de Broglie diz que o comprimento de onda de qualquer matéria é dada por
𝜆 = h / q ,
onde 𝜆 é o comprimento de onda de Broglie, h a constante de Planck, e q a quantidade de movimento. Esta expressão é conhecida como a equação de De Broglie.
Para átomos e moléculas, o comprimento de onda de Broglie é muito menor que a distância entre eles, sendo assim as moléculas não interagem como ondas entre si e sim como partículas.
Referências:
• GRIFFITHS, D. J. Introduction to quantum mechanics. 2.e d., Prentice-Hall, 2005.
• Robert Eisberg, Robert Resnick,.Quantum Physics of Atom, Molecules, Solids, Nuclei, and Particles, 2nd edition, John Wiley & Sons, 1985
• HEWITT, P. G., Conceptual Physics. 12 ed. San Francisco: Pearson Education, Inc., 2015.
Nenhum comentário:
Postar um comentário